国家药监局器审中心关于发布与抗肿瘤药物同步研发的原研伴随诊断试剂临床试验注册审查指导原则的通告
(2022年第28号)
发布时间:2022-06-28
为进一步规范伴随诊断试剂的管理,国家药监局器审中心组织制定了《与抗肿瘤药物同步研发的原研伴随诊断试剂临床试验注册审查指导原则》,现予发布。
特此通告。
附件:与抗肿瘤药物同步研发的原研伴随诊断试剂临床试验注册审查指 导原则
国家药品监督管理局
医疗器械技术审评中心
2022年6月28日
附件
与抗肿瘤药物同步研发的原研伴随诊断试剂
临床试验注册审查指导原则
一、前言
随着肿瘤生物学研究的进展,一些新的作用机制、作用靶点的抗肿瘤药物不断涌现,同时,临床实践中发现不同个体对同一药物的反应存在差异。宿主、肿瘤和外在因素会影响个体对抗肿瘤药物的反应。使用伴随诊断试剂检测肿瘤患者生物样本中生物标志物状态,能够为抗肿瘤药物的安全和有效使用提供重要信息;在抗肿瘤药物研发过程中,通过对疾病相关生物标志物的检测,有助于筛选出适合某类药物治疗的特定人群。部分抗肿瘤药物的开发过程会同步开发伴随诊断试剂,其临床试验尤其是其关键性临床试验过程会使用伴随诊断试剂。抗肿瘤药物临床试验既可以支持药物上市,亦可作为伴随诊断试剂伴随用途的确认证据支持其上市。同步开发过程中抗肿瘤药物及伴随诊断试剂如何共同开展临床试验是行业一直关注的问题。本指导原则旨在指导申请人开展与抗肿瘤药物同步研发的原研伴随诊断试剂临床试验及相关临床研究的注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。
本指导原则是针对伴随诊断试剂及抗肿瘤药物临床试验的一般要求,申请人应依据产品的具体特性确定其中内容是否适用。该文件为提供申请人和审查人员使用的指导性文件,不涉及注册审批等行政事项,亦不作为法规强制执行,如有能够满足法规要求的其他方法,也可采用,但应提供详细的研究资料。本指导原则是在现行法规体系及当前认知水平下制定的,随着法规的不断完善和科学技术的不断发展,本文件相关内容也将适时进行调整。
二、适用范围
以药物临床试验为时间节点可分为以下三种情况:
一是,在抗肿瘤药物的开发过程中同步进行伴随诊断试剂的开发,在药物临床前及临床研究过程中,通过与伴随诊断试剂共同验证确认,确定药物可能安全有效的治疗人群。抗肿瘤药物与伴随诊断试剂共同进行研究的数据作为二者上市的支持性证据。
二是,抗肿瘤药物临床试验中采用临床试验分析方法(Clinical Trial Assay,以下简称“CTA”)进行病例的生物标志物分析,相应的伴随诊断试剂开发相对滞后。基于CTA的设计,相关研发人员可以将其作为后续伴随诊断试剂开发的基础或作为后续该药物的候选伴随诊断试剂。
三是,如抗肿瘤药物在开发过程中,针对其伴随诊断试剂的需求有已上市产品,在进行充分的验证和确认的基础上,可选择已上市产品作为该药物的伴随诊断试剂,参与药物的研发过程。抗肿瘤药物及伴随诊断试剂的临床研究结果可作为药物上市及伴随诊断试剂变更的证据。
本指导原则适用于上述三种情况。如存在其他情况的,针对本指导原则的适用性,可与相关审评部门沟通。
三、伴随诊断试剂/CTA相关要求
伴随诊断试剂的性能直接影响抗肿瘤药物的疗效或相关不良反应,因此在抗肿瘤药物进行关键性临床研究时,应使用临床前性能已经充分验证的试剂。整个药物关键性临床研究中各机构应使用相同的检测试剂。在产品开发上,鼓励抗肿瘤药物与伴随诊断试剂共同开发同步申报,药品审评部门与医疗器械技术审评部门针对同步开发的药物和伴随诊断试剂协同审评,在双方对临床试验均认可的前提下,促使抗肿瘤药物与伴随诊断试剂同期上市。
临床试验中如使用CTA,应保证该方法学的性能及稳定性,一般而言,该方法的试剂组成、操作步骤、适用仪器、检测实验室应固定,且经过性能评估。临床试验过程中不建议使用多种分析方案、不同技术或缺乏跨实验室可再现的方法作为CTA,因为此类方法可能导致检测性能的变化以及检测结果之间缺乏可比性。如果抗肿瘤药物关键性临床试验过程中应用CTA,申请人应有进一步的伴随诊断试剂的研发计划,以确保抗肿瘤药物上市后能够科学、合理的应用于临床。
四、伴随诊断试剂临床性能研究
伴随诊断产品的临床性能最终会影响药物临床试验的有效性研究,为了尽量减少试剂对于人群检测的假阳性及假阴性,拟用于新药关键临床试验过程中的伴随诊断试剂,应在符合体外诊断试剂生产质量管理体系的条件下生产,且产品已经定型,并已完成相关的产品性能研究。相关研究包括主要原材料研究、生产工艺及反应体系研究、分析性能评估、能够满足临床验证的稳定性研究等。为了保证临床试验中伴随诊断试剂的质量,试剂申请人应在同步关键临床试验之前完成三批产品的检测报告。
(一)临床阳性判断值研究
伴随诊断产品阳性判断值是指临床治疗决策的界值(例如,检测结果高于阳性判断值的受试者可参加临床试验并接受治疗,而检测结果低于阳性判断值的受试者不能参加临床试验)。该值可能是检测限、定量限或具有临床意义的阳性判断值。
伴随诊断试剂阳性判断值的改变将影响临床试验的有效性结果。因此,在药物临床试验前应确定试剂的阳性判断值,根据该阳性判断值进行临床试验,不可随意调整。如药物临床试验中因伴随诊断试剂阳性判断值设定缺乏合理性导致药物临床试验失败则需要通过另一项临床试验来确认新的阳性判断值。
(二)试剂临床性能研究
伴随诊断试剂申请人应对产品的临床性能进行确认。建议申请人按照《体外诊断试剂临床试验技术指导原则》的要求,开展完整的临床试验以确认产品临床性能。临床试验设计可参考《抗肿瘤药物的非原研伴随诊断试剂临床试验注册审查指导原则》中关于伴随诊断试剂临床性能研究的要求。
如产品在检测过程中试验操作及结果判断较为复杂,容易受到不同操作人员、不同研究机构影响的情况下,建议申请人针对申报产品开展结果重现性研究,证明申报产品在不同检测条件下检测结果的一致性。
(三)使用已上市产品作为伴随诊断试剂
抗肿瘤药物可选择境内已上市的试剂作为新药的伴随诊断试剂开展临床试验。其适用人群、肿瘤类型、样本类型、检测目标物等应能够满足同步研发临床试验的要求。临床试验采用境内已上市的产品,在产品阳性判断标准等不发生变化的情况下,开展临床试验之前可不再进行产品性能研究、阳性判断值研究、临床性能等研究。已上市产品可通过变更注册增加新的药物伴随诊断的预期用途。同步开展的临床试验可以支持相关药物上市申请及伴随诊断试剂预期用途的变更申请。
五、同步研发临床试验
伴随诊断产品与抗肿瘤药物同步开发的临床试验,可为药物安全有效及伴随诊断产品的临床意义提供核心证据。该研究应为抗肿瘤药物安全有效的确证研究,一般为药物的III期或II期临床试验。此类试验通常以抗肿瘤药物有效性为主要目的,同时确认伴随诊断产品的伴随用途。药物临床试验过程中伴随诊断试剂的作用,包括作为药物临床试验过程中入组人群的筛选方法和作为药物临床试验过程中的生物标志物分层分析等。
(一)临床试验设计
抗肿瘤药物的临床试验设计首先需参考国家药监局发布的《抗肿瘤药物临床试验技术指导原则》。合理的临床试验设计可确认具有伴随诊断试剂的新药的安全性与有效性,通常为随机对照设计,特殊情况下可进行单臂设计的临床试验,还有其他诸如篮式设计、伞式设计等新型研究设计。
1.随机对照试验
1.1富集人群的随机对照研究
在伴随诊断试剂与抗肿瘤药物同步开展的临床试验中,依据伴随诊断试剂进行的富集设计的临床试验一般在受试者入组时,依赖于伴随诊断试剂的检测结果,符合某一生物标志物状态的人群入组至临床试验中,针对此部分人群开展临床研究。
富集设计的临床试验中,抗肿瘤药物疗效与伴随诊断试剂的临床意义直接相关,抗肿瘤药物疗效能够满足临床要求,则伴随诊断试剂临床意义明确。
1.2非富集人群的随机对照研究
在抗肿瘤药物临床试验设计过程中,如同步开发的伴随诊断试剂所检测生物标志物为前期已有充分的基础研究数据支持,但尚未经临床验证的生物标志物,由于不能确定该生物标志物与临床结果的相关性,通常应采用非标志物富集人群的临床试验。该临床试验在进行病例入组时,不依赖伴随诊断试剂进行病例的筛选,对于某一适应证的人群全部入组,同时,在临床试验中采用伴随诊断试剂根据生物标志物的状态进行分层分析。
在抗肿瘤药物疗效及伴随诊断临床意义评估时,应考虑试验组与对照组药效差异及试验组标志物阳性人群与标志物阴性人群药效差异。如基于事先良好的设计,研究有足够把握度证实目标人群能够从新药治疗中获益显著,则抗肿瘤药物适应证为此人群,同时,该临床试验亦能够确证伴随诊断的临床意义。
2.单臂试验(Single Arm Trial,SAT)
对于生物标志物阳性且无标准治疗或者罕见基因突变且相关药物疗效已经明确的晚期肿瘤患者,只有新药单药显示出了突破性的客观缓解率(ORR)和持久的缓解持续时间(DOR),才可以考虑以SAT作为关键注册临床试验,此时应选择独立评审委员会(IRC)评价的ORR作为主要研究终点并结合DOR、无进展生存期(PFS)和1年总生存期(OS)率等综合评价其临床获益。具体是否能够以单臂试验开展关键临床试验,申请人应参考已发布的《单臂试验支持上市的抗肿瘤药进入关键试验前临床方面沟通交流技术指导原则》,充分评估前期研究数据,并且与技术审评部门积极沟通交流。
在单臂试验作为抗肿瘤药物上市前关键性临床研究的情况下,伴随诊断试剂亦可考虑基于有限的病例数量基本认可其临床意义,进行附条件批准,待抗肿瘤药物上市后依据产品注册证中要求的确证性临床试验完成后,伴随诊断试剂注册人将该部分上市后资料在产品延续注册时递交,进一步确认其临床意义。如抗肿瘤药物上市后确证性临床试验涉及药物适应证变更的,伴随诊断试剂注册人应适时提交变更申请,同时,提供支持该变更的临床试验资料。
3.其他新型研究设计
随着肿瘤发生发展的分子机制研究的深入,肿瘤的精准诊断与靶向治疗已成为肿瘤治疗的重要手段。在肿瘤分子诊断过程中,一种肿瘤可能有多种分子分型或携带不同的突变基因,同时,不同的肿瘤可能携带相同的突变基因。在抗肿瘤药物临床试验设计上,出现了篮式试验与伞式试验等新的临床试验设计理念。
篮式试验是将带有相同靶点的不同肿瘤病例放进一个临床试验中进行抗肿瘤药物的研究,研究目的为某一个特定的靶向药物是否在所有或某些带有特定基因突变的肿瘤患者中有效。该设计在临床试验中研究多个瘤种,最终结果可能支持抗肿瘤药物在一个或几个瘤种中安全有效,伴随诊断试剂在临床试验过程中虽然检测了多个瘤种,其预期用途应为药物明确安全有效的肿瘤人群。参与篮式试验的伴随诊断试剂,其临床性能研究应能够涵盖该产品适用的不同肿瘤类型。
伞式试验是针对不同基因突变所致的同一肿瘤人群,将不同的靶点检测在同一时间里完成,然后根据不同的靶基因分配不同的精准靶药物,其目的是针对不同的突变状态的肿瘤患者,最终产生靶向治疗确定的证据。此种设计的临床试验,往往需要多个伴随诊断试剂或多个标志物联检的伴随诊断试剂进行病例的检测,而临床试验结果仅支持经过临床试验确认的治疗方式所对应的标志物检测的临床意义。参与伞式试验的伴随诊断试剂,其临床性能研究应能够涵盖所有标志物。
抗肿瘤药物临床试验设计涉及多个方面,关于临床试验设计过程中的其他要素,如主要终点选择、是否允许交叉、统计假设等均应遵循疾病发展过程的科学规律,并考虑药物进入体内发挥作用的过程,在此不再赘述,开展确证性试验前,请与监管部门沟通同步开发的试验设计。
(二)伴随试剂实施方案和要求
研究者应当在新药的试验方案及报告中以适当的方式明确伴随诊断试剂,伴随诊断试剂应明确从样本采集至报告检测结果全过程涉及的所有产品,临床试验中应明确伴随诊断试剂的作用。
(三)受试人群的选择
抗肿瘤药物与伴随诊断试剂同步开发的临床试验入组人群主要依据抗肿瘤药物临床适应证确定。筛选出的每个瘤种都需要确证其疗效和安全性。每个瘤种样本量应依据抗肿瘤药物疗效指标,按照统计学方法进行估算。
临床试验应能够确证药物在特定的目标人群中的安全性和有效性,评价肿瘤患者的临床获益情况。临床试验入组的人群应在探索性研究中观察到具有一定的疗效,还应考虑其他的影响因素:(1)肿瘤类型及分期;(2)疾病的分级、既往治疗或其他标准化的患者状况测量;(3)研究分层因素,如年龄、性别、种族、肿瘤大小、体力状况等。
药物临床试验过程中,一般按照临床试验方案要求对入组病例进行生物标志物检测,标志物检测所用样本一般为前瞻性采集的样本。如采用生物标志物作为入组标准,可使用富集设计对标志物特定状态进行富集,确保足够数量的受试者入组,以满足临床评价的要求。
生物标志物不作为入组标准时,人群入组除了应满足抗肿瘤药物临床试验受试者入组标准,还需考虑待分析人群中标志物的阳性率,临床试验需保证具有各标志物状态的人群能够评价抗肿瘤药物的有效性与安全性。对于能够评估标志物表达程度的伴随诊断试剂,临床试验入组病例时应考虑表达不同标志物的病例均有一定的样本量。
在某些特殊的情况下,针对入组病例无法获得前瞻性采集样本时,也可采用病例的既往留存样本,采用此种方式入组的人群应避免因选择病例留存样本而产生偏倚。不能在设定标准之外富集或缺失具有某一特征的病例。
(四)疗效评价
同步研发的临床研究主要是评价新药的临床获益情况,依据药物的获益从而证实伴随诊断试剂的作用。支持药物批准上市的疗效终点指标通常是显示临床获益的证据,直接的生存证据如OS,或其他替代终点如PFS、ORR等。申请人应根据所研究的药物类别、肿瘤类型、当前临床治疗状况以及开发目标等来综合考虑,选择适当的主要和次要疗效指标。有关各终点指标选择的考虑请参见《抗肿瘤药物临床试验终点技术指导原则》。
(五)统计分析
基于抗肿瘤药物与伴随诊断试剂同步开发的临床试验设计,一般而言,针对抗肿瘤药物疗效相关统计分析同样能够确认生物标志物临床意义。如临床试验未采用标志物富集入组的策略,临床试验中为了确认受试药物对某一特定人群是否有效,应进一步依据病例样本中标志物的状态对病例进行分层分析,具体的分层方法需在试验方案或统计分析计划中阐明。标志物分层分析的结果应能够体现伴随诊断试剂的临床意义。
(六)临床试验资料要求
同步开发的临床试验资料主要包括临床试验方案及临床试验报告等,支持伴随诊断试剂临床意义的药物临床试验资料应与药品申请人递交药品审评部门的资料一致。该部分资料可由试剂申请人作为伴随诊断试剂临床试验资料进行提交,或由药物申请人按照《国家药监局关于医疗器械主文档登记事项的公告》(2021年第36号)进行主文档登记,试剂申请人在递交申报资料时应对该主文档文件进行关联。
1.伴随诊断试剂介绍
临床试验告中应明确伴随诊断试剂的基本信息,根据方案中提供的伴随诊断试剂信息应能够对应至申报的伴随诊断试剂。临床试验应明确适用样本类型,适用样本可为新鲜样本或冻存样本,样本的保存条件应满足伴随诊断试剂说明书的要求。
临床试验应明确样本信息,包括但不限于以下几个方面,(1)样本类型,例如FFPE组织、新鲜组织、冰冻组织、血液等;(2)肿瘤样本的肿瘤百分比/基质/坏死比例;(3)潜在的抑制物或交叉反应物的含量,例如黑色素;(4)收集样本的解剖学部位;(5)肿瘤类型:原发性、转移性;(6)样品采集方式:如手术取材或细针穿刺等;(7)样本的保存及运输条件等。
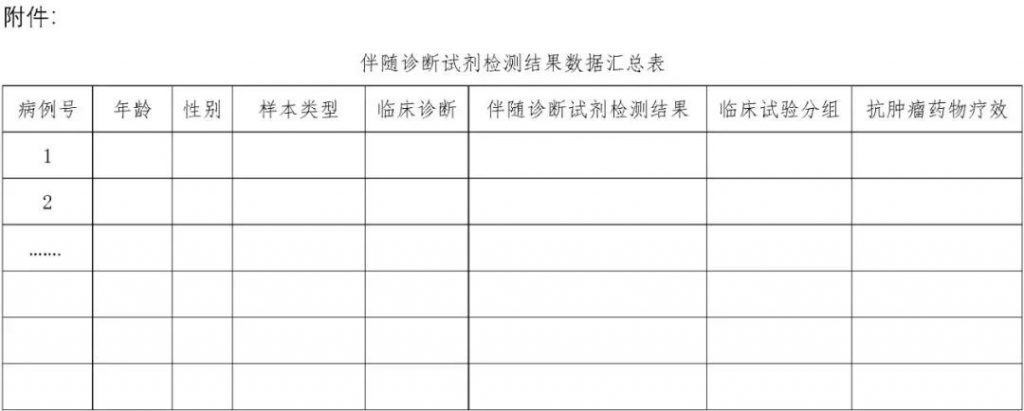
2.临床试验数据汇总表
同步开发临床试验建议以列表的形式对伴随诊断试剂检测结果进行汇总,数据汇总表应包括以下内容:受试者编号、年龄、性别、样本类型、病例临床背景信息、伴随诊断试剂检测结果、临床试验分组、抗肿瘤药物疗效,具体形式可参考附件。病例的背景信息应明确患者肿瘤类型、分期、既往治疗方案等内容,病例临床评价终点建议参考《抗肿瘤药物临床试验终点技术指导原则》。采用标志物富集设计的临床试验中,对于未入组至临床试验的病例,数据汇总表可不体现临床试验分组及病例临床试验终点的内容。数据汇总表可由伴随诊断试剂申请人进行汇总。
3.临床试验报告附件
抗肿瘤药物与伴随诊断试剂同步开发的临床试验资料中,伴随诊断试剂申请人应将相关伴随诊断试剂和抗肿瘤药物说明书作为附件提交。
4.伴随诊断试剂临床意义的支持性证据基于全部的抗肿瘤药物关键性临床研究。如抗肿瘤药物在审评过程中药品审评部门要求其进一步补充相关资料,则伴随诊断试剂申请人在提交药物临床试验资料时,应将药物临床试验需要补充的资料一并提交。
5.资料签章要求
药物临床试验资料相关签字、签章应满足药品审评相关资料递交要求。此外,药品生产企业提交的抗肿瘤药物临床试验资料应有药品生产企业签章。
六、采用CTA进行临床试验相关要求
如药物临床临床试验采用CTA进行生物标志物分析,应充分考虑生物标志物检测的样本类型、收集方法、处理和保存方式及保存时间、实验操作过程的规范化对生物标志物检测的影响。建立一个样本采集、储存和评估的统一标准操作流程(SOP),以保证生物标志物检测结果的稳定性。
抗肿瘤药物临床试验病例采用CTA进行生物标志物分析,申请人应明确后续伴随诊断试剂的开发计划。后续开发的伴随诊断试剂应进行临床性能研究及伴随诊断临床意义研究,临床意义研究应采用桥接试验的路径。关于临床性能研究及桥接试验的相关要求,建议参考《抗肿瘤药物的非原研伴随诊断试剂临床试验注册审查指导原则》相关要求。
七、产品说明书
抗肿瘤药物及伴随诊断试剂说明书中相关内容应与二者共同研发的临床试验保持一致。
(一)伴随诊断试剂说明书要求:
1.预期用途
伴随诊断试剂预期用途应依据抗肿瘤药物与伴随诊断试剂同步开发的临床试验确定,依据临床试验中得出的药物适应证,确定相关伴随诊断试剂的预期用途,应明确检测结果的临床意义,即能够指导某一治疗类产品的应用,预期用途应包括:肿瘤类型、样本类型、标志物状态、药物名称等内容。伴随诊断试剂的预期用途应与相关抗肿瘤药物适应证相对应。如:抗肿瘤药物奥希替尼与人EGFR T790M检测试剂同步开发的临床试验证明奥希替尼适用证为:用于既往经表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI)治疗时或治疗后出现疾病进展,并且经检测确认存在 EGFR T790M 突变阳性的局部晚期或转移性非小细胞性肺癌(NSCLC)成人患者的治疗。对应人EGFR T790M检测试剂预期用途确定为该产品用于检测非小细胞性肺癌(NSCLC)成人患者FFPE组织中EGFR T790M 突变,用于患者使用奥希替尼治疗的伴随诊断。如适应症发生变化,应提供相应的临床试验证据进行变更申请。
2.产品说明书中阳性判断值应与同步开发的临床试验中伴随诊断试剂所用阳性判断值一致。
3.伴随诊断试剂说明书中产品性能指标部分应有抗肿瘤药物与伴随诊断试剂同步开发的临床试验总结,包括:临床试验设计、入组人群、样本量、人口学分析、疾病特征分析、不同标志物分层中的药物药效等。
(二)抗肿瘤药物说明书要求
1. 适应证
抗肿瘤药物说明书中仅在适应证或用法用量项下描述为药物的使用需结合由国家药品监督管理局批准的伴随诊断试剂的检测结果。
如奥希替尼:一线使用本品治疗前必须明确有经国家药品监督管理局批准的EGFR基因检测方法检测到的EGFR19外显子缺失突变或21外显子L858R置换突变阳性的患者。对于既往经EGFR-TKI治疗时或治疗后出现疾病进展的患者,使用本品治疗前必须明确有经国家药品监督管理局批准的检测方法检测到EGFR-T790M突变。
帕博利珠单抗:帕博利珠单抗适用于由国家药品监督管理局批准的检测评估为PD-L1肿瘤比例分数(TPS)≥1%的表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性的局部晚期或转移性非小细胞肺癌一线单药治疗。
2.临床试验
建议申请人在产品说明书中临床试验部分载明抗肿瘤药物与伴随诊断试剂的同步研发的临床试验相关内容,包括:临床试验设计、入组人群、样本量、人口学分析、疾病特征分析、不同标志物分层中的药物药效、临床试验过程中所用伴随诊断试剂等。
八、接受境外临床试验数据
国家药品监督管理局针对药品和医疗器械分别发布了《接受药品境外临床试验数据的技术指导原则》和《接受医疗器械境外临床试验数据技术指导原则》。伴随诊断试剂临床试验包括产品临床性能研究及伴随诊断临床意义研究两方面,本指导原则重点讨论伴随诊断临床证据的接受境外临床试验试验数据的考虑。
对于抗肿瘤药物与伴随诊断试剂在境外同步开发的临床试验和包括中国在内的国际多中心临床试验,在满足上述指导原则的基础上可作为支持抗肿瘤药物和伴随诊断试剂境内上市的临床资料。以下分别介绍伴随诊断试剂与抗肿瘤药物接受境外临床试验数据的考量。
(一)伴随诊断试剂接受境外临床试验数据
1.同步开发临床试验境内外使用同一伴随诊断试剂
针对全球多中心临床试验中各临床试验机构使用同一伴随诊断试剂及全球多中心临床试验和中国境内临床试验各临床试验机构使用同一伴随诊断试剂的情况,针对伴随诊断试剂临床意义的证据为药品审评部门认可的支持该药物上市的临床试验证据。
2.同步开发临床试验境内外使用不同的伴随诊断试剂
针对全球多中心临床试验中国境内外使用伴随诊断试剂不同及中国拓展临床试验与全球多中心临床试验使用伴随诊断试剂不同的情况,对于申报中国境内同步开发的伴随诊断试剂,虽然抗肿瘤药物临床试验能够满足药物上市的条件下,但境内伴随诊断试剂的临床规模可能不足以支持其上市。试剂申请人应将该试剂与境外药物临床试验中所用的试剂进行桥接试验,该部分试验可以在境外或境内完成。桥接试验的结果可支持该试剂上市。
3.在药效学数据能够满足评价产品临床意义的前提下,针对进口产品应评估该类产品在境内应用是否存在临床试验条件的差异,如医疗环境、医疗设施、研究者能力等。如存在差异,应针对差异内容在中国境内开展临床试验(如PD-L1的结果重现性研究等)。
(二)抗肿瘤药物接受境外临床试验数据
境外临床试验数据用于我国药品注册申请的,应提供境外临床试验的完整数据,试验数据符合ICH 临床试验管理规范(GCP)的相关要求,并与我国GCP 规范要求相一致。同时需对有效性、安全性、种族敏感性进行分析。具体条件请参考《接受药品境外临床试验数据的技术指导原则》,并需与药品审评中心就具体数据进行沟通交流。
(三)其他
境外进行的抗肿瘤药物与伴随诊断试剂同步开发的临床试验如能够满足本指导原则的要求,但临床试验方案及报告中未明确伴随诊断试剂相关信息,应由出具临床试验报告的相关机构或主要研究者出具相应的补充文件。
九、其他
抗肿瘤药物与伴随诊断试剂共同开发的,申请人在产品开发及申报过程中应考虑同步进行,监管部门在产品审评过程应考虑协同审评,努力做到药物与相关伴随诊断试剂协同审批上市。
(一)建议抗肿瘤药物与伴随诊断试剂在产品开发阶段同步进行,伴随诊断试剂在同步开发临床试验开展之前,可根据产品临床应用进行设计开发或更新,以满足抗肿瘤药物伴随诊断的用途,最终以定型的产品与药物同步进行临床确认。
(二)如抗肿瘤药物按照《药品注册管理办法》,纳入突破性药物治疗程序或优先审批程序,与该药物共同开发的伴随诊断试剂在产品注册过程中可申请按照《医疗器械优先审批程序》进行优先审批。
(三)抗肿瘤药物在上市后其适应证发生涉及生物标志物的变更后,相关伴随诊断试剂生产企业应根据变更情况向医疗器械技术审评部门申请该产品预期用途的变更。
十、起草单位
国家药品监督管理局医疗器械技术审评中心。
合作单位:国家药品监督管理局药品审评中心。
十一、参考文献:
1.《体外诊断试剂注册与备案管理办法》(国家市场监督管理总局令第48号),2021年8月26日。
2.《药品注册管理办法》(国家市场监督管理总局令第27号),2020年3月30日。
3.《体外诊断试剂临床试验技术指导原则》(国家药品监督管理局通告2021年第76号),2021年9月28日。
4.《抗肿瘤药物临床试验技术指导原则》 (原国家食品药品监督管理局公告2012年第122号),2012年5月15日。
5.《抗肿瘤药物临床试验统计学设计指导原则》(国家药监局药审中心通告2020年第61号),2020年12月31日。
6.《药物临床试验富集策略与设计指导原则(试行)》(国家药监局药审中心通告2020年第60号),2020年12月31日。
7.《单臂试验支持上市的抗肿瘤药进入关键试验前临床方面沟通交流技术指导原则》(国家药监局药审中心通告2020年第47号),2020年12月2日。
8.《接受药品境外临床试验数据的技术指导原则》(国家药品监督管理局2018年第52号),2018年7月10号。
9.《接受医疗器械境外临床试验数据技术指导原则》(国家药品监督管理局2018年第13号),2018年1月11号。
10.《基因组生物标志物、药物基因组学、遗传药理学、基因组数据和样本编码分类的定义》(ICH指南E15)
11.《药物或生物技术产品开发相关的生物标记物:资格认定申请的背景资料、结构和格式》(ICH指南E16)。
12.《In Vitro Companion Diagnostic Devices,Guidance for Industry and Food and Drug Administration Staff》(美国食品药品监督管理局),2014年8月6日。
13.《Principles for Codevelopment of an In Vitro Companion Diagnostic 2Device with a Therapeutic Product,Draft Guidance for Industry and Food and Drug Administration Staff》(美国食品药品监督管理局),2016年7月15日。
14. 斯蒂芬奈德尔. 抗肿瘤药物设计与发现 [M].北京:化学工业出版社,2020。
来源:
国家药品监督管理局医疗器械技术审评中心 2022年06月28日

