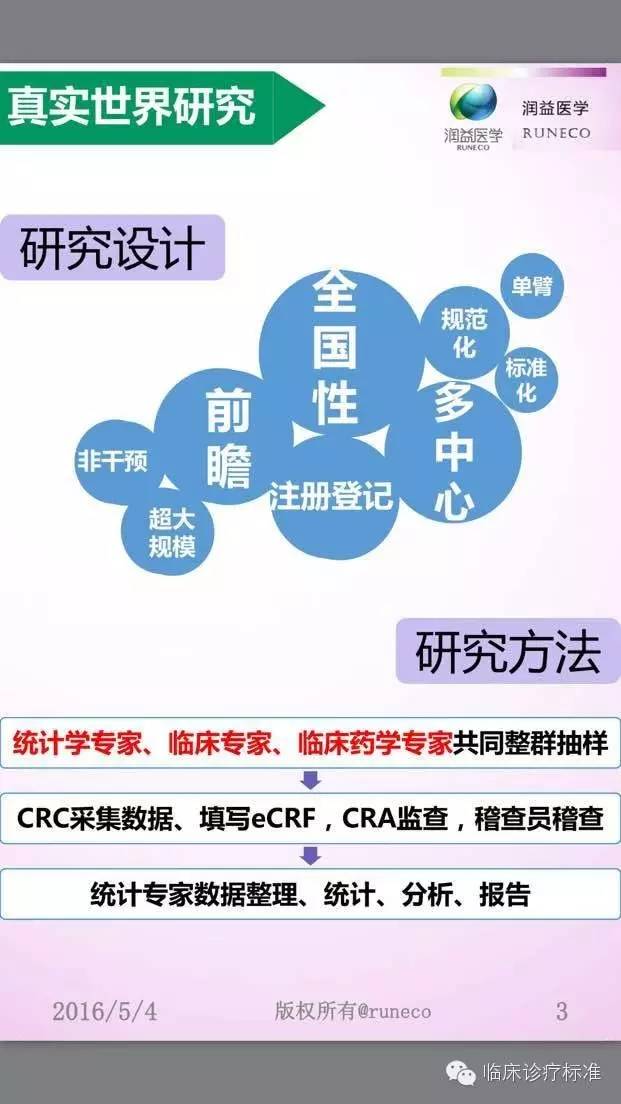
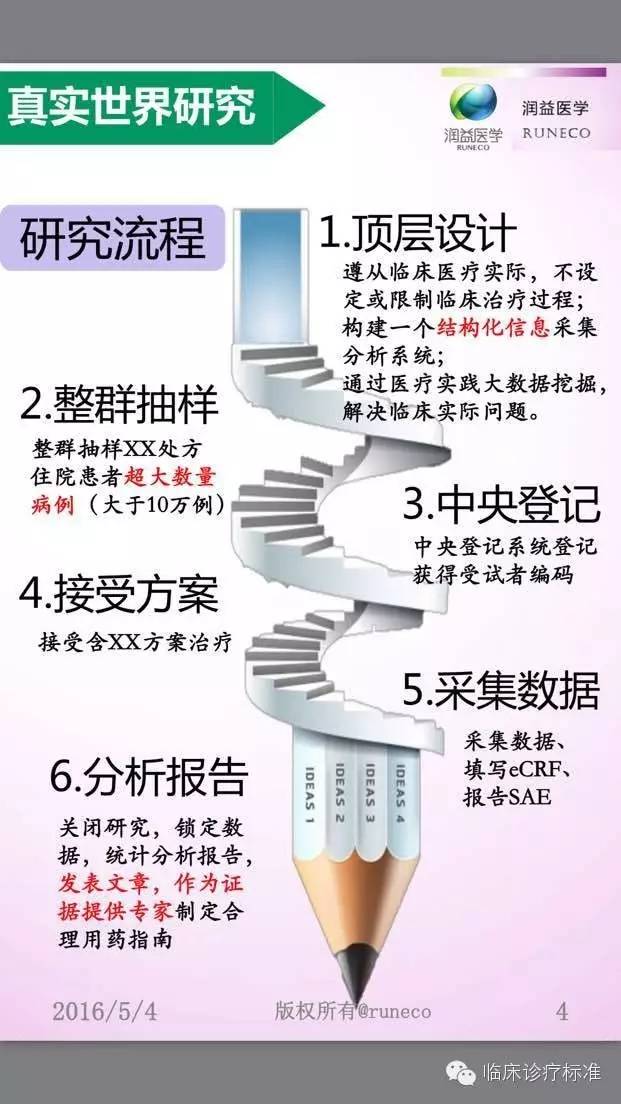
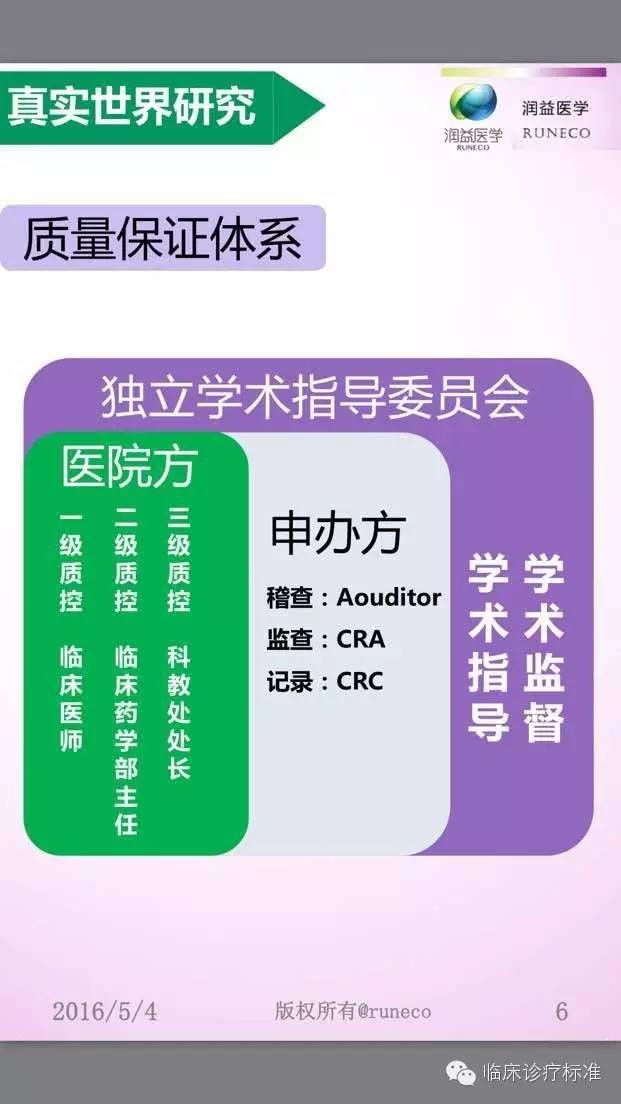
什么是真实世界研究? 与随机对照研究、单病例随机对照试验等,RWR 的区别是什么呢?RWR又有哪些分类呢?
人类医学史上第一个临床研究是JamesLind对柠檬酸治疗坏血的研究,而第一个文献报道的随机对照试验(RCT)是有现代医学随机对照试验之父Austin Bradford Hill的“四环素治疗肺结核”的研究。长久以来,RCT被医学界认为是“理性疗法(rationaltherapeutics)”,但RCT在实际临床研究中存在真实性差、外推困难等问题逐渐被研究者重视。在这样的背景下,RWR愈发获得研究者的关注。


RWR起源于实用性临床试验,最早应用于药物流行病学范围。指在较大的样本量(覆盖具有代表性的更广大受试人群)的基础上,在真实医疗过程中,根据患者的实际病情和意愿非随机选择治疗措施,开展长期评价,并注重有意义的结局治疗,在广泛真实医疗过程中评价干预措施的外部有效性和安全性。
RWR涵盖的范围较RCT更广,除治疗性研究之外,还可用于诊断、预后病因等方面的研究。RWR的目的旨在获得更符合临床实际的证据,使研究结果更易转化到临床实践中。与RCT相比,RWR涵盖的范围更广,除治疗性研究之外,还可用于诊断、预后病因等方面的研究。 RCT所获得的是试验性数据,RWR所获得的是真实数据。RCT需要回答的问题是“是否有效和安全”;RWR所回答的问题是“能否有效作为医疗手段”。
表1 真实世界研究与随机对照研究对比
真实世界研究(RWR) | 随机对照研究(RCT) | |
目标 | 效果研究 | 效力研究 |
时间 | 长 | 短 |
时间及方案设计 | 根据不同研究目标和内容选择设计方案 | 试验性方法为主,类试验为辅 |
质量控制手段 | 非随机、开放性、不使用安慰剂的非盲试验 | 随机分配、盲法、标准化治疗,可使用安慰剂 |
纳入和排除标准 | 较宽泛纳入标准和较少的排除标准 | 严格的纳入和排除标准 |
样本量和代表性 | 样本量偏小则产生偏差,样本量为考察结果真实性的重要指标 | |
干预 | 真实治疗 | 标准化治疗 |
结局测量指标 | 多采用有广泛临床意义的指标:病死率、复发率、伤残程度、生活质量 | 多以一个或者一些特定病症或体征为评价目标 |
数据采集、管理及统计分析方法 | 二者都强调应严格控制数据采集、管理和分析过程,所采用的统计学方法学方法基本相同,如卡方检验、Fisher检验、log-rank检验、ROC曲线、Kaplan-Meier生存曲线; | |
伦理 | 受试者不会接受没有任何效能的治疗,更易满足伦理学要求,不存在干预等问题,故伦理学原则不会对研究时间、样本量等因素产竽制约 | 受试者损害最小化原则,为避免过多的受试者接受可能疗效较差的治疗或发生不良反应,充分保证受试者的权益,伦理学要求在进行RCT前计算样本量,确定具有检验效能和得出良好可信度估计值的最小样本量 |
局限性 | 样本量巨大,成本相对昂贵,数据处理难 | 外推性较差 |
表2 真实世界研究与单病例随机对照试验比较
真实世界研究 | 随机对照试验 | 单病例随机对照试验 | |
样本量 | 大 | 根据试验设计 | 最少 |
随机对象 | 不随机 | 受试者 | 干预措施 |
成本 | 昂贵 | 低 | 低 |
那么RWR都包括哪些类型呢?RWR包括临床效果研究,经济效益研究、流行病学研究以及患者回馈调查。
①临床效果研究 (观察代表临床效果的医疗指征),这种研究可以观察多个临床介入手段的实际效果,也可以观察多个时间段的变化,多个地区之间的区别,以及在某种设定条件下的实际临床效果;
②经济效益研究(评估为达到相同程度临床效果所需要的资源),这种研究考量的是一个医疗手段(例如新药、手术方法、诊断方法等)对管理某病种的常规预算所产生的影响(budget impact),这种影响可以由资源节省或资源利用等概念来显示;
③流行病学研究 (观察在某种条件下的原发病发病率,并发症发病率,发病或病情蔓延影响因子等);
④患者回馈调查研究(了解患者对某些治疗手段的直感反应,包括症状效果、副作用、便利性、生活质量指数等),在一定规范条件下执行的患者回馈研究(patient reported outcomes)结果可以经包括美国食品与药物管理局这样的药物审批机构认可,列为新药的特征之一。
↓↓↓ 下面分享 润益医学 制作的关于真实研究的珍贵材料
法迈生医学参与全球首个抗肿瘤药(艾迪注射液)10万例真实世界临床研究
江苏法迈生医学科技有限公司与贵州益佰制药股份有限公司2016年3月达成战略合作,共同开展10万例艾迪注射液上市后安全性再评价真实世界的研究。法迈生医学承担该研究中的整群抽样、受试者注册登记、数据采集、数据管理、基本统计分析、撰写总结报告等工作。